Tout ce que vous devez savoir sur le cancer de la prostate
L’Imagerie par Résonance Magnétique multiparamétrique
L’Imagerie par Résonance Magnétique multiparamétrique (IRMmp) est indubitablement l’avancée majeure de ces 2 dernières décennies dans la prise en charge du cancer de la prostate.
• Une technologie à base d’aimants
La technologie IRM n’est pas basée sur l’utilisation des rayons X et de ce fait est moins invasive que le scanner. En effet, l’IRM utilise des électro-aimants superconducteurs qui produisent un champ magnétique capable d’aligner dans la même direction les particules d’hydrogène (60% du corps humain est constitué de molécules d’H2O) de chaque cellule de la zone explorée. Cependant, lorsque le tissu est pathologique, les atomes d’hydrogène au sein de ce tissu vont perdre cette capacité d’alignement. Quand les électro-aimants sont inactivés, chaque atome d’hydrogène retourne à sa position initiale, et ce faisant émettre une certaine quantité d’énergie variable en fonction du statut normal ou anormal du tissu où il se trouve. Cette énergie est ensuite détectée par une antenne qui transmet cette information à un ordinateur sous la forme d’un signal. En dernier lieu, un logiciel convertit les signaux en images qui seront interprétées par un radiologue. Au long d’un examen IRM, différentes séquences sont produites dont certaines nécessitent une injection de gadolinium afin de mieux mettre en évidence certaines structures anatomiques. Contrairement au scanner qui ne produit que des plans axiaux du corps humain, l’IRM est capable de générer des coupes dans n’importe quel axe. Habituellement sont analysés les axes transversal (tête vers pied), sagittal (de droit à gauche) et coronal (d’avant en arrière).
• Les séquences
Lors d’une IRMmp, 3 séquences sont nécessaires : la séquence axiale T2 (T2W), celle de diffusion (DWI = diffusion weighted imaging) et une dernière après injection nommée Dynamic Contrast Enhanced (DCE). Pour une interprétation radiographique de la maladie, les acquisitions de ces différentes séquences expliquent le caractère multiparamétrique de l’IRM. Les acquisitions des plans doivent être superposables afin de pouvoir comparer les différentes séquences pour une zone donnée. Habituellement, le temps nécessaire pour une IRMmp est de 30 à 45 minutes.
-
La séquence axiale T2 (T2W)
La séquence T2W est avant tout morphologique avec une haute résolution permettant une analyse anatomique fine. Bien que l’IRMmp implique l’acquisition des 3 plans axial, sagittal et coronal, le plus souvent les coupes axiales restent les plus utilisées pour le diagnostic mais aussi les biopsies ciblées. En situation normale, les zones périphérique et antérieure montrent un hypersignal (zone plus claire) tandis qu’une lésion cancéreuse dans la zone périphérique apparaîtra plutôt en hyposignal (zone plus sombre) avec des limites floues (image 19). Dans la zone transitionnelle, la présence de nodules adénomateux bénins rendent l’interprétation radiologiques plus difficiles.
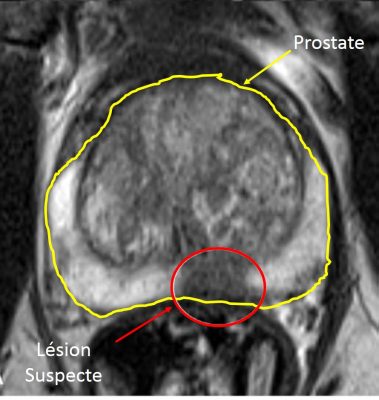
Image 19 : Séquence T2 axiale ou T2W (avec l’aimable autorisation du Pr P De Visschere – Gent)
-
Séquence de diffusion (DWI)
Contrairement à la séquence T2W, DWI est une séquence fonctionnelle et non morphologique. Dans cette séquence DWI, la lésion cancéreuse apparaît en hypersignal (zone plus claire) comparée à du tissu normal (image 20). En lien avec la séquence DWI, le coefficient apparent de diffusion (ADC) est basé sur le calcul entre 2 séquences DWI prises dans des conditions techniques différentes. L’intérêt de l’ADC qui apparaît comme un hyposignal est qu’il est inversement proportionnel à l’agressivité du cancer se traduisant par une corrélation négative entre l’ADC et la classification ISUP (score d’agressivité du cancer).
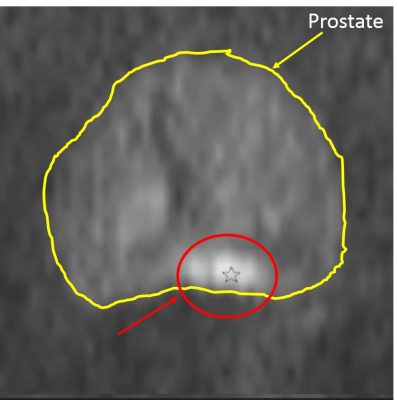
Image 20 : Séquence DWI dite de diffusion (avec l’aimable autorisation du Pr P De Visschere – Gent)
-
Séquence injectée (DCE)
La séquence DCE est réalisée après injection d’un produit de contraste qui est le plus souvent du gadolinium ou un chélate de magnesium. Des produits naturels tels que la myrtille ou le thé vert ont été utilisés pour certaines séquences. Des acquisitions successives permettent de mettre en évidence un réhaussement de contraste précoce dans les lésions suspectes liées à la présence de la néo-angiogenèse (nouveaux vaisseaux anormaux). Les lésions de cancer de la prostate apparaissent sous forme d’un hypersignal comparé au tissu environnant (image 21). Cette fois encore, l’interprétation des images est plus facile dans la zone “homogène” périphérique que dans la zone transitionnelle adénomateuse. L’absence de réhaussement ne permet pas d’exclure définitivement la présence d’un cancer et plus généralement une séquence DCE devrait toujours être interprétée de manière concomitante de séquences T2W et DWI. En effet, il n’est pas de réhaussement de contraste en DCE montrant une lésion cancéreuse qui ne soit confirmée par des séquences T2W et/ou DWI anormales.
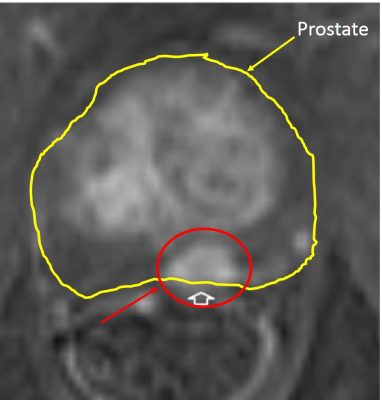
Image 21 : Séquence DCE dite de perfusion (avec l’aimable autorisation du Pr P De Visschere – Gent)
• PIRADS classification
Inspirée de la classification sur le cancer du sein BI-RADS (Breast Imaging and Reporting Archiving Data System), la Société Européenne de Radiologie Urogénitale (ESUR) a proposé des recommandations basées sur un consensus pour l’IRMmp nommées PI-RADS. Selon la localisation de la lésion suspecte en zone périphérique ou transitionnelle, le calcul du score PI-RADS se fait de façon différente. Cette classification va de 1 à 5, 1 représentant l’absence de lésion et 5 le plus haut degré de suspicion (figure 2 et image 22). En 2014, une mise à jour de la première version du score PI-RADS a mené à la classification PI-RADS v2. Plus la lésion est agressive (score PI-RADS plus élevé), meilleur est le taux de détection même pour des tumeurs de petits volumes (tableau 4).
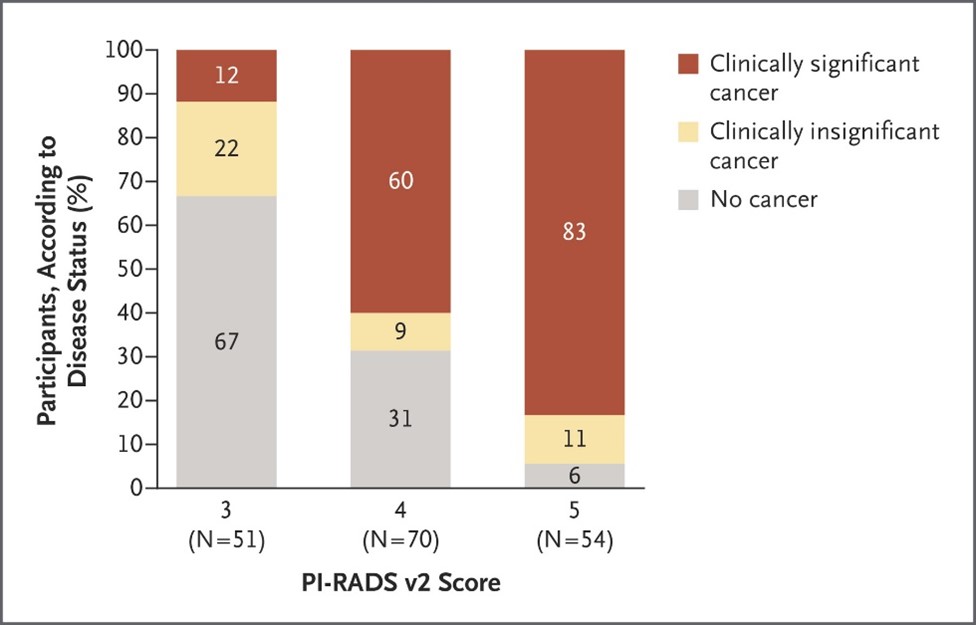
Figure 2 : Risk of prostatic cancer depending on the PI-RADS v2 score (source : EAU guidelines)
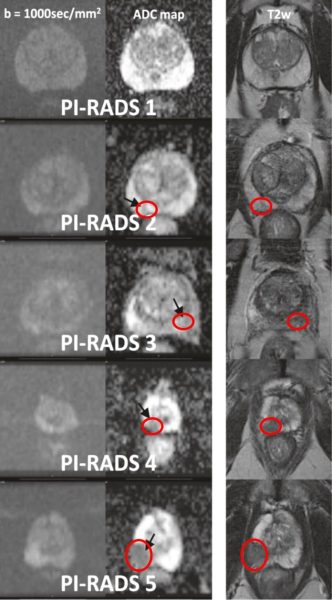
Image 22 : Illustration de la classification PIRADS allant de 1 à 5 (avec l’aimable autorisation du Dr P. Steiger – Klinik Beau-Site)
Ces dernières années, la détection du cancer de la prostate a été l’objet de progrès constants (tableau 4). Les avancées technologiques telles que l’utilisation d’électro-aimants superconducteurs plus puissants permettant de passer de 1.5 à 3 Tesla (3T) ont montré que les progrès à venir surmonteront sans aucun doute les difficultés techniques actuelles et permettront de détecter les plus petits cancers avec une précision redoutable. Dans certains centres, des IRM 7T sont déjà en fonction procurant par exemple des images cérébrales d’un degré de qualité inégalé tandis que des IRM 10.5T sont déjà à l’étude dans le domaine de la recherche (image 23).
Image 23 : Un électro-aimant superconducteur avec une résolution spatiale de l’ordre de 0.1 mm comparée à 1 mm actuellement
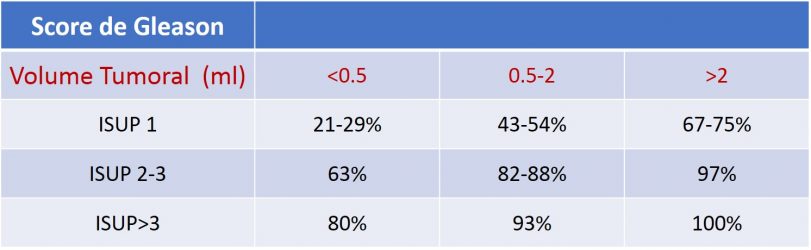
Tableau 4 : Taux de détection par IRM du cancer de prostate en fonction du volume tumoral et de la classification ISUP (agressivité du cancer) (source : recommandations EAU 2020)


