Adjuvante und/oder palliative Behandlungen
Behandlungen > Adjuvante und/oder palliative Behandlungen
Adjuvante und/oder palliative Behandlungen
Die folgenden Behandlungen werden entweder als mögliche kurative Strategien eingesetzt, oft in Kombination mit einer Strahlentherapie als Teil einer multimodalen Behandlung, oder häufiger als palliative Option in einem späteren Stadium der Erkrankung. Mit Ausnahme der Hormontherapie und des Mitoxantrons beruhen die anderen Strategien auf wissenschaftlichen Erkenntnissen hinsichtlich des Einflusses auf das Überleben (Bild 72). Diese sogenannten systemischen Behandlungen unterscheiden sich von lokalisierten Behandlungen, da sie im ganzen Körper wirken und sich ausbreiten, während kurative oder palliative lokalisierte Behandlungen durch physikalische Einwirkung (chirurgische Ablation, Bestrahlung oder z. B. Laser) auf ein definiertes Ziel wirken.
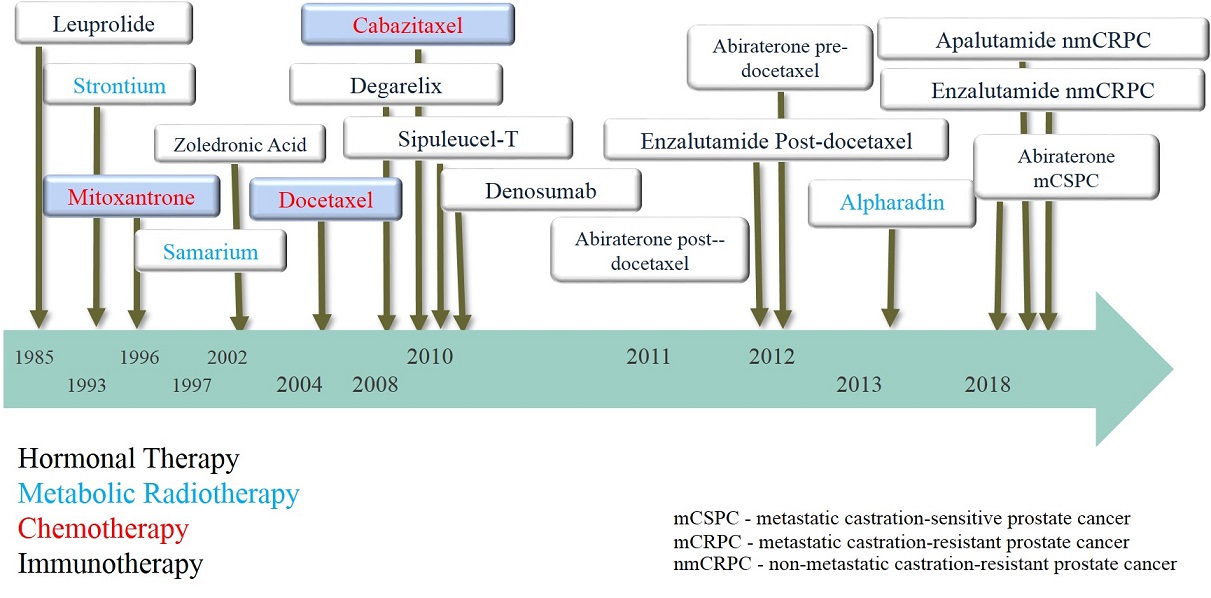
Bild 72 : Meilensteine der systemischen Behandlung bei fortgeschrittenem Prostatakrebs
Hormontherapie
Die Androgendeprivationstherapie (ADT) bei Prostatakrebs ist die älteste systemische Behandlung, die es gibt. Sie wurde 1941 von C. Huggins veröffentlicht und brachte ihm 1966 den Nobelpreis für Medizin ein (Bild 73). Sie basiert auf der Hormonabhängigkeit des Prostatakrebses, wobei Androgene ein wesentlicher Treibstoff für das Wachstum und die Progression der Krebszellen sind. Beim Mann werden Androgene zu 95 % von den Hoden und zu den restlichen 5 % von den Nebennieren produziert. Die Produktion von Testosteron hängt von der Hypothalamus-Hypophysen-Achse ab, wobei erstere das luteinisierende Hormon Releasing Hormon (LH-RH) produziert, das die Produktion des luteinisierenden Hormons (LH) durch letztere anregt. LH stimuliert die Produktion von Androgenen durch die Hoden [Leydig-Zellen] (Bild 74). Der Hypothalamus steuert die Hypophyse durch intermittierende Sekretion von LH-RH.
Lange Zeit wurde die ADT nur durch die beidseitige Entfernung des Hodens (Orchiektomie) erreicht. Später, 1980, wurde der erste LH-RH (auch GnRH genannt) Agonist (d.h. Leuprolid, Goserelin oder Triptorelin) verwendet, um eine chemische Kastration zu erreichen. Die Wirkung der intramuskulären Injektion dauerte zunächst 1 Monat, dann 3 Monate und erreichte 6 Monate nach dem Jahr 2000. Es könnte seltsam erscheinen, einen LH-RH-Agonisten zu injizieren, der auf natürliche Weise die Produktion von Androgenen durch den Hoden stimuliert, um eine hormonelle Deprivation zu erreichen. Der Trick liegt jedoch in dem natürlichen intermittierenden hypothalamischen Rhythmus der LH-RH-Sekretion, der durch die Injektion komplett unterbrochen wird und stattdessen LH-RH kontinuierlich ausgeschüttet wird. Neben den üblichen Nebenwirkungen wie Hitzewallungen, starke Beeinträchtigung der Sexualfunktion, Verlust von Muskelmasse und Müdigkeit ist einer der Nachteile der LH-RH-Agonisten das Aufflammen zu Beginn der Behandlung. In der Tat wird die Injektion in den ersten 2 oder 3 Wochen eher die Testosteronproduktion erhöhen, was zu einem möglichen klinischen Fortschreiten der Krankheit führt. Um den Flare-up-Effekt zu vermeiden, wird in der Regel eine ergänzende hormonelle Behandlung mit Anti-Androgenen (z. B. Bicalutamid oder Flutamid) im gleichen Zeitraum durchgeführt.

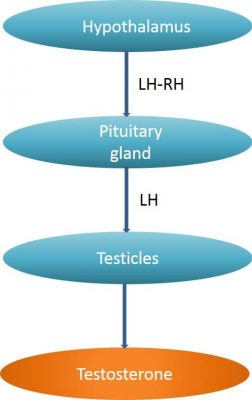
Bild 74 : Die Hypothalamus-Hypophysen-Achse
Eine weitere Möglichkeit, den Flare-up-Effekt zu vermeiden, ist die Verwendung eines LH-RH-Antagonisten anstelle eines Agonisten. Allerdings wurde erst 2008 der erste LH-RH-Antagonist (Degarelix) zugelassen. Aus galenischen Gründen erfordert es eine monatliche Injektion.
Die Hormontherapie wird hauptsächlich als erster Schritt einer palliativen Strategie eingesetzt, um das Fortschreiten der Erkrankung zu reduzieren, wobei sie im Allgemeinen eine gute Wirkung auf vorhandene Metastasen hat. Meistens ist der Prostatakrebs tendenziell hormonsensitiv (HSPC), was bedeutet, dass die Krankheit in diesem Stadium auf ADT anspricht. Nach einer gewissen Zeit wird der Prostatakrebs hormonresistent (CRPC = castration resistant prostate cancer). In diesem fortgeschrittenen Stadium ist die Hormontherapie weniger oder gar nicht wirksam und es sind andere systemische Behandlungen erforderlich, um das Fortschreiten des Krebses zu verhindern. Wenn der Krebs hormonresistent wird, wird die ADT trotz begrenzter wissenschaftlicher Beweise nie abgesetzt. In jüngerer Zeit wurde die Hormontherapie in multimodale Strategien in Kombination mit externer Strahlentherapie im sogenannten Bolla-Protokoll aufgenommen. Diese multimodale Strategie basiert auf der Synergie zwischen der biologischen Wirkung der Hormontherapie und der physikalischen Wirkung der Strahlung auf die Prostatakrebszellen (siehe Validierte Therapie – Externe Strahlentherapie).
Die jüngste Innovation auf dem Gebiet der Hormontherapie bei Prostatakrebs ist die Perspektive des oralen LH-RH-Antagonisten ” relugolix “, der den Vorteil hat, die Therapie im Bedarfsfall schnell zu beenden.
Chemotherapie
Mit Ausnahme von Mitoxantron, das keinen Einfluss auf das Überleben bei fortgeschrittenem Prostatakrebs hatte, wurde die Chemotherapie erst 2004 zu einer validierten Behandlung auf dem Gebiet des Prostatakrebses. Bis zu diesem Zeitpunkt war kein Onkologe auf dem Gebiet des Prostatakrebses tätig. Urologen kümmerten sich um ihre Patienten von einem sehr frühen Stadium bis zu einem fortgeschrittenen und metastasierten Stadium. Die erste Anwendung der Chemotherapie bei Prostatakrebs war für CRPC-Patienten. Bei Prostatakrebs wird die Chemotherapie immer intravenös verabreicht und erfordert oft die Platzierung eines Ports, eines Katheters, der ein kleines medizinisches Gerät ist, das unter die Haut der rechten Brust gelegt wird (Bild 75).
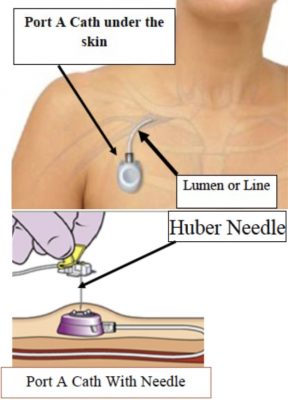
Bild 75 : Port eines Katheters an der rechten Brust
Die erste zugelassene Chemotherapie bei metastasiertem Krebs war Docetaxel, das in TAX327 eine bescheidene Verbesserung des Gesamtüberlebens um 2,5 Monate zeigt [37]. Im Jahr 2010 wurde dann Cabazitaxel, ebenfalls aus der Familie der Taxane, zugelassen, das ebenfalls das Überleben leicht verlängert (2,4 Monate) [38]. Anschließend wurde Docetaxel bei HSPC-Patienten evaluiert und zeigte eine höhere Verlängerung des Überlebens auf fast 14 Monate im Vergleich zur alleinigen ADT. Bei hochvolumigen Erkrankungen war der Unterschied im Überleben mit 17 Monaten sogar noch größer [39].
In Bezug auf die Chemotherapie werden sowohl Docetaxel als auch Cabazitaxel als Zweitlinientherapeutika eingesetzt, wenn ein HSPC hormonresistent wird, und die Zugabe von Docetaxel zur ADT wird als Erstlinientherapie bei HSPC eingesetzt.
Zielgerichtete Therapien
Zielgerichtete Therapien sind die letzte therapeutische Innovation auf dem Gebiet des fortgeschrittenen Prostatakrebses. Sie sind das Ergebnis jahrzehntelanger Forschung in der Molekularbiologie und der Entdeckung von intrazellulären molekularen Zielen, die durch neue Substanzen blockiert werden könnten. Zielgerichtete Therapien werden oral verabreicht.
- Neue Androgen-gerichtete Strategien
Zwei neue Moleküle stellen die neuen Hormontherapien für fortgeschrittenen Prostatakrebs dar, Abirateronacetat und Enzalutamid, die 2011 bzw. 2013 zugelassen wurden (Bilder 76 und 77). Abirateron hat eine starke Wirkung auf den Androgenrezeptor (AR) und Enzalutamid hemmt CYP-17, ein Enzym, das für die Androgensynthese benötigt wird. Diese neuen Androgentherapien sind für die Erst- und Zweitlinienbehandlung von metastasierten CRPC-Patienten nach einer Chemotherapie indiziert [40-43]. Wenn eine dieser beiden Behandlungen versagt, spricht die andere schlecht an.

Bild 76 : Molekularstruktur von Abirateronacetat
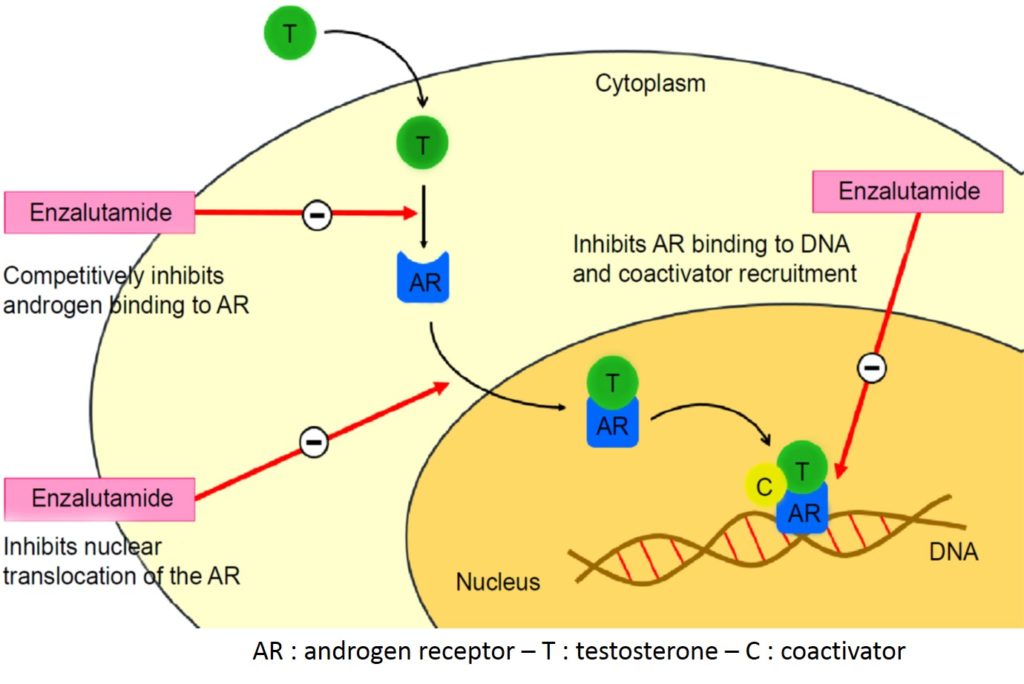
Bild 77 : Wirkmechanismus von Enzalutamid im Androgenrezeptor-Signalweg (Quelle: angepasst aus Rodriguez-vida A. et al. Drug Design, Development and Therapy 2015)
- PARP-Hemmer
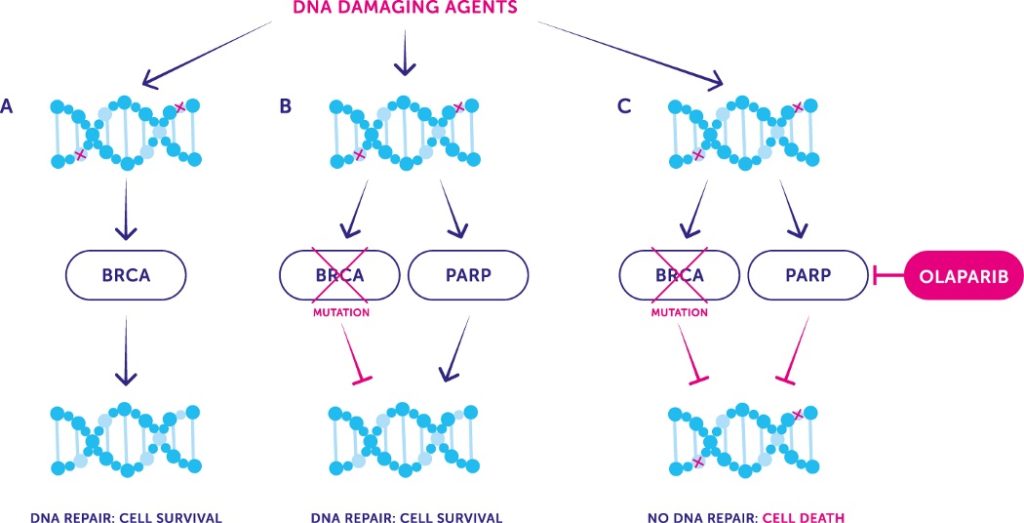
Bild 78 : PARP-Inhibitor blockiert den MMR-Systemweg, was zum Absterben von Tumorzellen führt (Quelle : Cancer UK)
Immuntherapie
Die Immuntherapie ist ein onkologischer Therapieansatz, der darauf abzielt, das Immunsystem wiederherzustellen, um Krebszellen abzutöten. Sie wirkt hauptsächlich auf Immunzellen (T-Zellen), die auf die Zerstörung von Krebszellen spezialisiert sind.
- Pembrolizumab
Pembrolizumab ist ein monoklonaler Antikörper, der wie Olaparib ebenfalls auf das MMR-System abzielt, jedoch auf eine andere Weise. Krebszellen haben nämlich die Fähigkeit, Liganden (PD-L1 [Program Death Ligand 1] und PD-L2) zu produzieren, die an den Rezeptor der T-Zellen des Immunsystems binden, um diese zu inaktivieren. Indem sie an den Rezeptor binden, blockieren die PD-L1- und PD-L2-Liganden die Immunantwort der T-Zellen, die normalerweise darauf programmiert sind, die Krebszellen abzutöten (Bild 79). Pembrolizumab konkurriert mit PD-L1 und PD-L2 und hat eine höhere Affinität zum PD1-Rezeptor. So hilft Pembrolizumab, die T-Zell-Immunantwort wiederherzustellen (Bild 80). Im Jahr 2017 wurde Pembrolizumab für ausgewählte metastasierte CRPC-Patienten mit Mutationen im MMR-System zugelassen.

Bild 79 : Inaktivierung einer T-Zelle durch Bindung von PD-L1- und PD-L2-Liganden an den PD-1-Rezeptor (Quelle : www.keytrudahcp.com)
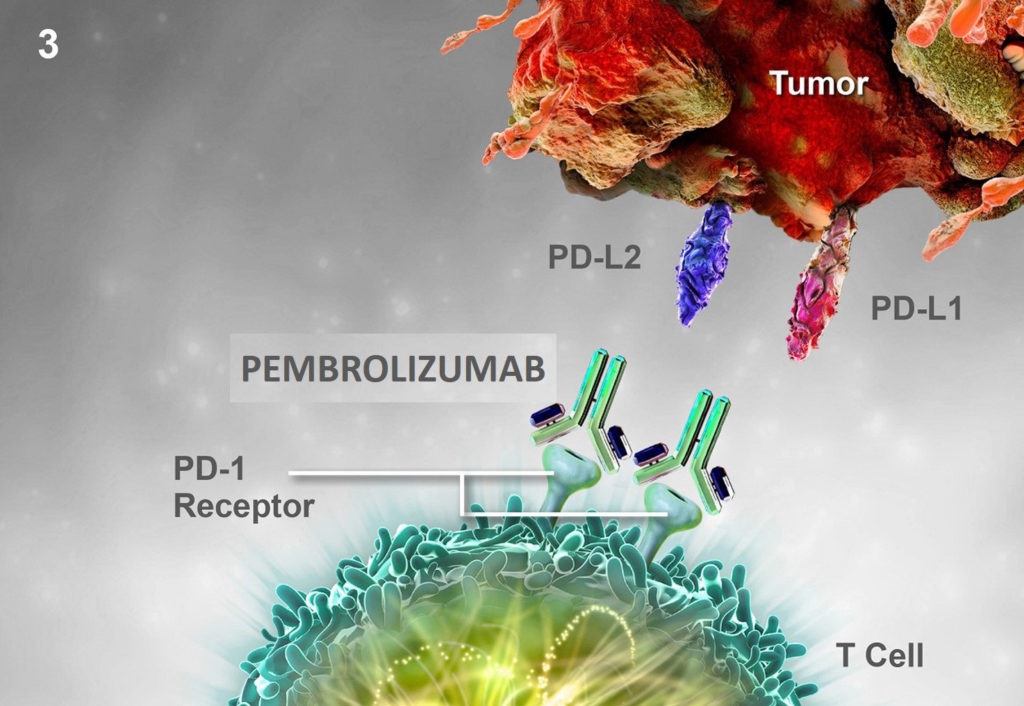
Bild 80 : Kompetitive Bindung von Pembrolizumab an den PD-1-Rezeptor, wodurch die Interaktion mit PD-L1 und PD-L2 blockiert und die T-Zell-Immunantwort wiederhergestellt wird (Quelle : www.keytrudahcp.com)
- Sipuleucel-T
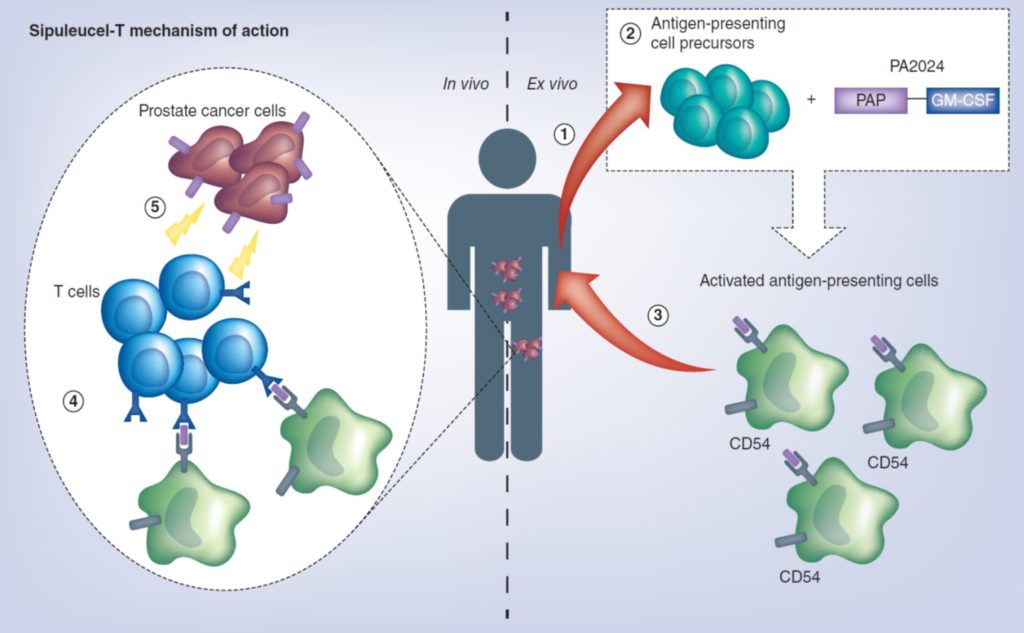
Bild 81 : Wirkmechanismus von Sipuleucel-T (Quelle : Handy CE and Antonarakis ES. Future Oncol. 2018)


