Traitements Validés
Traitements > Traitements Validés > Radiothérapie Externe
Aspects scientifiques du traitement
Impulsée, en Allemagne, par le Pr W. Roentgen, la radiothérapie a été initiée au tout début du 20ème siècle. La radiothérapie externe (EBRT) se base sur l’usage de différentes sortes de rayonnements selon le type de cancer, sa localisation profonde ou superficielle et également son volume plus ou moins important. En outre, le tissu au sein duquel le cancer s’est développé est un élément important du fait d’une résistance plus ou moins grande aux irradiations. Ainsi la résistance aux rayons du cerveau est bien supérieure à celle du testicule. Contrairement à la radiothérapie dite interstitielle où le rayonnement provient de sources temporaires ou permanentes placées au sein de l’organe cible, la radiothérapie externe ne s’exerce que par une source externe et distante. Les radiations sont générées par différents types d’équipements tels que des générateurs à rayons X (X-rays), à Cobalt-60 [Ɣ-rays] (image 42), des accélérateurs linéaires ou LINAC (rayons X à haute énergie ou électrons), et plus rarement des émetteurs à protons ou neutrons.

Image 42 : La radiothérapie externe au Cobalt-60 par le Theratron Junior utilisé dans les années 50.
- Mécanisme d’action
Le but des radiothérapies est de briser les brins d’ADN au sein des cellules de manière si intense qu’elle rend impossible toute réparation de ce dernier par le système idoine (Système de Réparation des Mésappariements = SRM) qui permet, en temps normal, de restaurer le matériel nucléaire. Ce bombardement moléculaire entraîne la mort des cellules cancéreuses appelée apoptose et à un moindre degré des cellules normales avoisinantes qui gardent une capacité plus importante de régénération. Les effets secondaires délétères de la radiothérapie sont précisément liés à la proportion de cellules normales atteintes par les rayons administrés.
Les différentes modalités thérapeutiques d’irradiation
- La radiothérapie conformationnelle 3D (3D-CRT)
La radiothérapie conventionnelle bidimensionnelle est une ancienne technique où les traitements étaient planifiés à partir d’un nombre de faisceaux limités par un simple plan orthogonal sous la forme d’un carré ou d’un rectangle. La faible conformité offerte par cette approche engendrait des effets secondaires conséquents car les organes adjacents (vessie, rectum) se retrouvaient intégrer dans le champ à haute dose d’irradiations. A contrario, la radiothérapie conformationnelle tridimensionnelle (3D-CRT) est basée sur la prise en considération des volumes anatomiques fournis le plus souvent par un scanner. Cette approche en 3D permet aux champs d’irradiation de mieux mouler ou se « conformer » au volume cible en évitant autant que ce peut les tissus sains avoisinants. Les volumes cibles sont définis en 3 dimensions utilisant des contours dessinés à l’aide de coupes successives sur la base d’une analyse scanographique (image 43). Il s’agit d’une procédure à plusieurs étapes incluant le positionnement du patient, sa stricte immobilisation, l’acquisition des images, la définition des volume cible, des champs d’irradiation ainsi que le calcul des doses. Le principal avantage de la 3D-CRT est la possibilité de l’escalade de dose tout en contrôlant la toxicité des tissus avoisinants. Cependant cette technique reste lente et demande un travail conséquent.
- La radiothérapie avec modulation d’intensité (IMRT)
La radiothérapie avec modulation d’intensité (IMRT) est une forme avancée de 3D-CRT et représente le type de radiothérapie externe la plus utilisée actuellement. Une technologie innovante produit une distribution de doses plus uniformes avec toujours le même objectif : intensifier l’irradiation au niveau de la tumeur et réduire la toxicité avoisinante. Des programmes de fluence sont transmis électroniquement à un accélérateur linéaire dirigé par ordinateur afin de délivrer des faisceaux avec modulation d’intensité. En utilisant plus de 9 angles différents et des milliers de segments, il permet une escalade de doses accrues sur les cellules cancéreuses les plus agressives (image 44). Les modalités principales d’IMRT sont la radiothérapie guidée par l’image (IGRT) utilisant des images en temps réel durant la procédure en lieu et place d’une acquisition pré-procédurale, et la radiothérapie dite arcthérapie (VMAT) basée sur un arc complet d’unités d’irradiation sur 360°.
- La radiothérapie stéréotaxique (SBRT)
D’une technologie encore plus poussée, la radiothérapie stéréotaxique repose davantage sur les dernières connaissances issues du domaine de la biologie. Le rationnel est le lien entre l’irradiation et les effets cytotoxiques où un nombre réduit de doses d’irradiation plus conséquentes ont un effet de destruction cellulaire supérieure à une dose globale équivalente délivrée en un nombre de fois plus important. Dans ce cadre, une thérapie complète durera 1 à 5 jours au lieu de plusieurs semaines. La technique SBRT est aussi le fruit de progrès technologiques avec le développement du Gamma Knife®, X-Knife®, CyberKnife® et Clinac® (image 45).
Les radiothérapies externes dans leur ensemble sont des traitements validés connaissant des progrès permanents dont le dernier est l’hypofractionnement. En effet le fractionnement standard initial de 1.8-2 Grays nécessite 5 séances par semaine pendant 6-7 semaines. Puis l’hypofractionnement conventionnel de 3-5 Grays est également réalisé 5 jours par semaine mais seulement sur 2 semaines consécutives. Enfin, avec la radiothérapie SBRT atteignant un hypofractionnement de 15-25 Grays, 1 à 5 séances suffisent.
- Protonthérapie/Neutronthérapie
Au lieu de rayons X, la thérapie par faisceau de protons projette des protons sur la zone cible. Contrairement aux rayons X qui délivrent de l’énergie avant et après avoir touché leur cible, les protons causent peu de dommage aux tissus qu’ils traversent. Bien qu’en théorie la protonthérapie soit plus efficace que les rayons X, à ce jour les études n’ont pas démontré la véracité de cette approche. Très peu de centres dans le monde sont capables de fournir ce traitement très honéreux. Contrairement aux autres radiothérapies, la protonthérapie tout comme la neutronthérapie n’ont pas été étudiées sur de larges populations et des données scientifiques supplémentaires sont nécessaires.
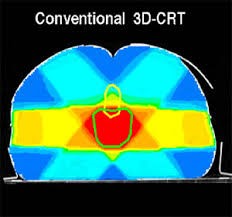
Image 43 : Champs d’irradiation lors d’une radiothérapie conformationnelle 3D (3D-CRT)
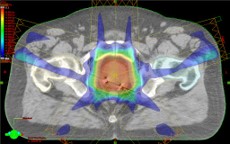
Image 44 : Champs d’irradiation lors d’une radiothérapie avec modulation d’intensité (IMRT)
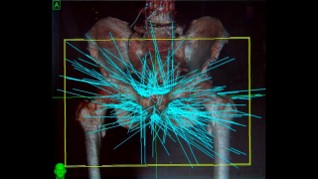
Image 45 : Champs d’irradiation lors d’une radiothérapie stéréotaxique (SBRT)
La Radiothérapie externe et l’hormonothérapie : une combinaison gagnante
Basés sur des données expérimentales, des radiothérapeutes tels que le Pr M. Zelefsky et A. d’Amico aux Etats-Unis, et M. Bolla en Europe ont évalué l’intérêt d’un traitement combiné associant l’hormonothérapie (HT) et la radiothérapie externe (HRT) dans des populations de patients à risque intermédiaire et à haut risque [14-16]. L’ensemble des études sur ce sujet ont confirmé la supériorité de l’HRT sur l’EBRT seule en particulier concernant les patients de risque intermédiaire et de haut risque tel que mentionné dans les recommandations suivantes.
Indications/Recommandations
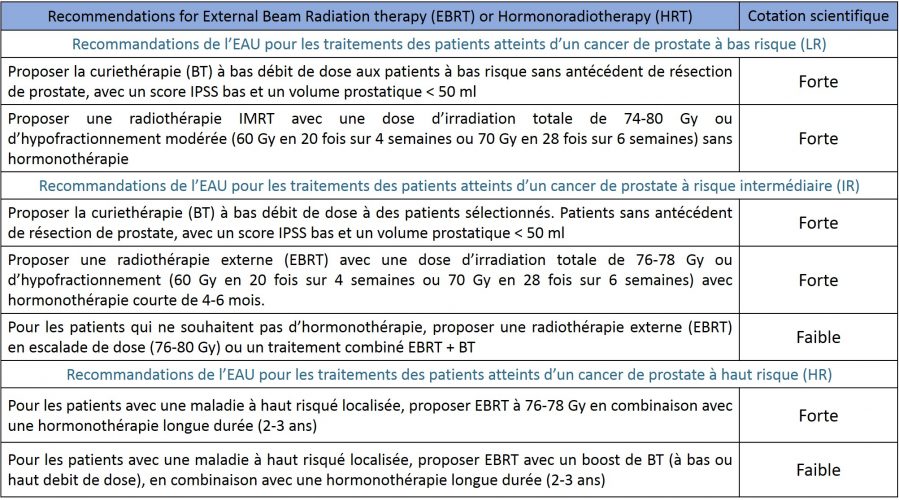
Sur la base d’innombrables études scientifiques, les sociétés savantes publient régulièrement des recommandations afin de standardiser au mieux la prise en charge du cancer de la prostate. Les plus importantes associations d’Urologie, européenne (EAU), américaine (AUA), chinoise (CAU), la Confederacion Americana de Urologia en Amérique Latine sont largement en phase sur les indications de radiothérapie externe. A l’exception du cancer de la prostate à bas risque où le surtraitement touche encore de trop nombreux patients, il est communément admis pour les cancers de la prostate localisés et davantage encore dans les formes localement avancées que la radiothérapie externe et l’hormonoradiothérapie sont des traitements validés voire les traitements de référence. Il est important de préciser que l’hormonothérapie n’a pas d’indication pour les cancers à bas risque alors qu’une hormonothérapie de 6 mois est recommandée pour les patients de risque intermédiaire et de 2-3 ans pour ceux à haut risque (tableau 10).
Résultats
Sur la base de solides études scientifiques, la radiothérapie externe a montré depuis longtemps son efficacité tant dans les cancers de la prostate localisés que localement avancés voire dans certaines situations de cancers métastatiques ganglionnaires limitées au bassin. Dans ces 2 dernières situations, la radiothérapie externe associée à l’hormonothérapie est considérée comme le traitement de référence. En effet, la chirurgie d’ablation (prostatectomie radicale) représente la méthode la plus adaptée tant que la maladie est limitée à l’organe avec une délimitation anatomique précise mais beaucoup plus délicate lorsque le cancer a franchi la capsule prostatique. En revanche, la radiothérapie externe, peut facilement et avec beaucoup plus de précision englober un champ d’irradiation sensiblement plus large que la prostate comprenant l’ensemble de la zone tumorale à détruire. Dans ces situations de cancers localement avancés, les rayons X ou Ɣ sont de meilleurs outils thérapeutiques que la précision d’un bistouri. Avec une escalade de doses se situant entre 75 et 80 Grays, le taux de rémission se situe aux alentours de 70-75% à 5-10 ans de suivi ce qui signifie qu’un patient sur 3-4 récidivera de son cancer. Du fait de l’escalade de dose, la toxicité des tissus environnants est accrue aux alentours de 25-30%.
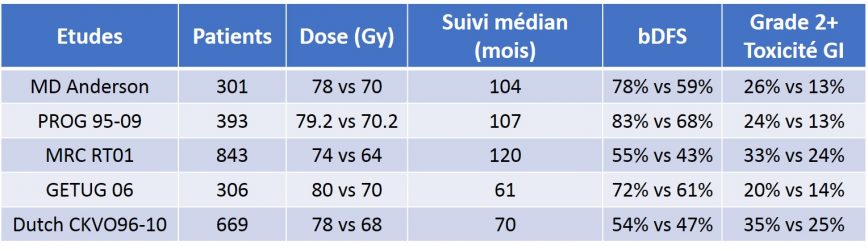
Tableau 11 : Résultats de l’efficacité et de la toxicité des principaux essais cliniques randomisés en radiothérapie externe


